A história do mercado de doenças raras nos últimos anos tem se centrado na descoberta e lançamento de novas moléculas. Embora muitos desenvolvedores de medicamentos para doenças raras tenham sido tradicionalmente empresas menores do exterior, as grandes farmacêuticas estão começando a enxergar mais promessas nesse espaço à medida que os acordos e aquisições dessas pequenas empresas inovadoras se multiplicam.
Recentemente a Biogen adquiriu a fabricante de medicamentos para doenças raras Reata Pharmaceuticals, que obteve a aprovação da FDA para seu medicamento Skyclarys para a ataxia de Friedreich em março, por US$ 7,3 bilhões. Já a Alexion da AstraZeneca aumentou seu investimento em doenças raras ao comprar o portfólio de terapia genética em estágio inicial da Pfizer por aproximadamente US$ 1 bilhão.
No início deste ano, a Novartis também adquiriu a Chinook Therapeutics, focada em distúrbios renais raros, por US$ 3,2 bilhões. E, no maior negócio de biotecnologia de 2022, a Amgen comprou a Horizon Therapeutics por US$ 27,8 bilhões em dezembro para expandir seu portfólio de doenças raras.
No meio de tantos negócios e do crescente interesse no setor, as aprovações de novos medicamentos para doenças raras dispararam. Entre 2015 e 2022, os medicamentos para doenças raras representaram metade de todas as aprovações da FDA. No Brasil, o aumento expressivo no número de registros de tratamentos para doenças raras iniciou-se em 2016 com pico 2019. Desde 2016 a média de registros concedidos para medicamentos destinados para doenças raras tem sido de 27 registros por ano.
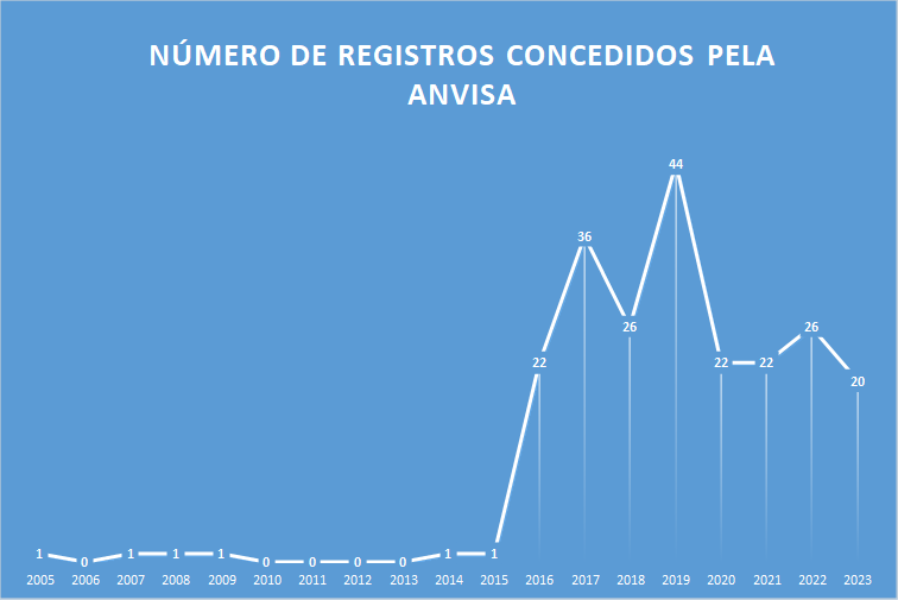

A relação atualizada de todas as empresas e medicamentos com registro aprovado para tratamento de doenças raras no Brasil pode ser consultado neste link.
Inúmeros desafios ainda persistem nesse campo das doenças raras como dificuldades na seleção de pacientes para ensaios clínicos, mudanças no cenário regulatório e complexidades nas estruturas de incentivo para essa área. Entretanto, é evidente que as empresas têm investido cada vez mais recursos na pesquisa e desenvolvimento desse tipo de medicamento e a expectativa é que mais opções de tratamentos sejam lançadas nos próximos anos.
Referências:
Agência Nacional de Vigilância Sanitária – Anvisa
Food and Drug Administration – FDA
Imagem: FarmaNetwork





