A garantia da qualidade é uma questão crítica na indústria farmacêutica. A contaminação por partículas visíveis em medicamentos injetáveis é uma preocupação que tem impactos diretos na saúde dos pacientes e na reputação dos fabricantes. O artigo Visible Particulate Contamination Control for Injectable Products: A Life-Cycle Approach, publicado no PDA Journal of Pharmaceutical Science and Technology explora em detalhes esse tema.
O artigo discute sobre a importância de se adotar uma abordagem de ciclo de vida para o controle eficaz da contaminação por partículas visíveis em produtos injetáveis, destacando a necessidade de uma estratégia abrangente que atue desde o desenvolvimento do produto até sua fabricação e inspeção.
A autora Stephen Langille começa ressaltando que a qualidade de produtos farmacêuticos vai além da sua eficácia terapêutica, abrangendo também a disponibilidade do produto para os pacientes. Produtos farmacêuticos injetáveis devem estar livres de contaminantes químicos, microbiológicos e físicos, incluindo partículas visíveis que podem afetar a segurança do paciente e a qualidade do produto. A presença de tais partículas pode não apenas representar um risco direto para o paciente, mas também indicar problemas no processo de fabricação que afetam a segurança, qualidade, pureza ou potência do produto.
A falha na prevenção e detecção de contaminação por partículas visíveis pode ter implicações sérias para a disponibilidade do produto. Lotes rejeitados ou recolhidos devido à contaminação por partículas visíveis podem resultar em perdas financeiras significativas para os fabricantes, além de afetar a confiança dos pacientes nos produtos farmacêuticos e perda de reputação. Isso ressalta a necessidade de um rigoroso programa de controle de contaminação por partículas visíveis, que englobe todos os estágios do ciclo de vida do produto.
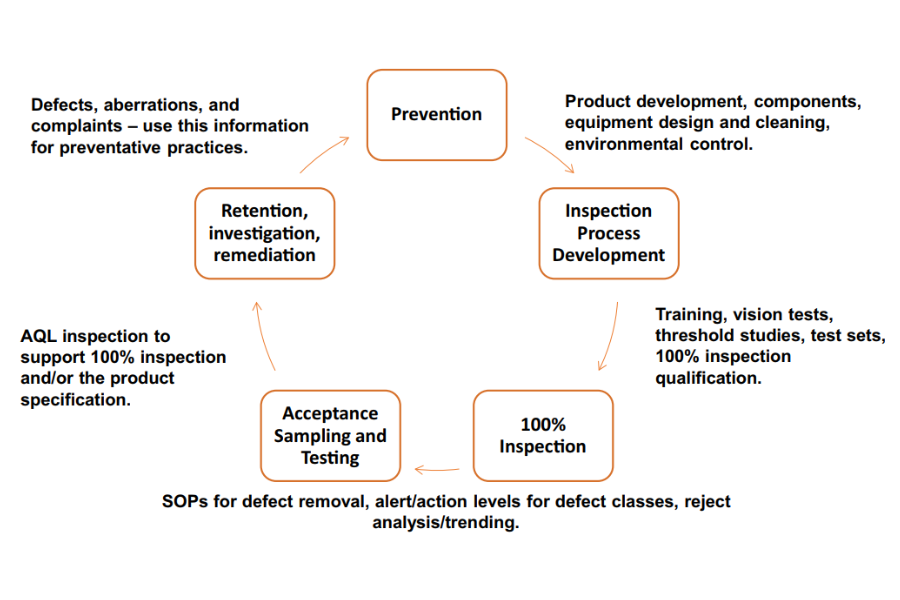
Figura 1: Modelo de ciclo de vida para controle de partículas visíveis. Fonte: Langille, S. E., PDA Journal of Pharmaceutical Science and Technology.
Um aspecto fundamental da abordagem de ciclo de vida é a implementação de um processo de inspeção de 100% para detectar partículas visíveis. Esse processo começa durante o desenvolvimento do produto, levando em consideração suas características, tipo de recipiente, método de inspeção e o tipo de defeito que o método pretende detectar. O artigo destaca que, em alguns casos, produtos difíceis de inspecionar, como produtos liofilizados ou embalados em recipientes opacos, podem exigir testes destrutivos complementares para atender aos requisitos de controle de contaminação.
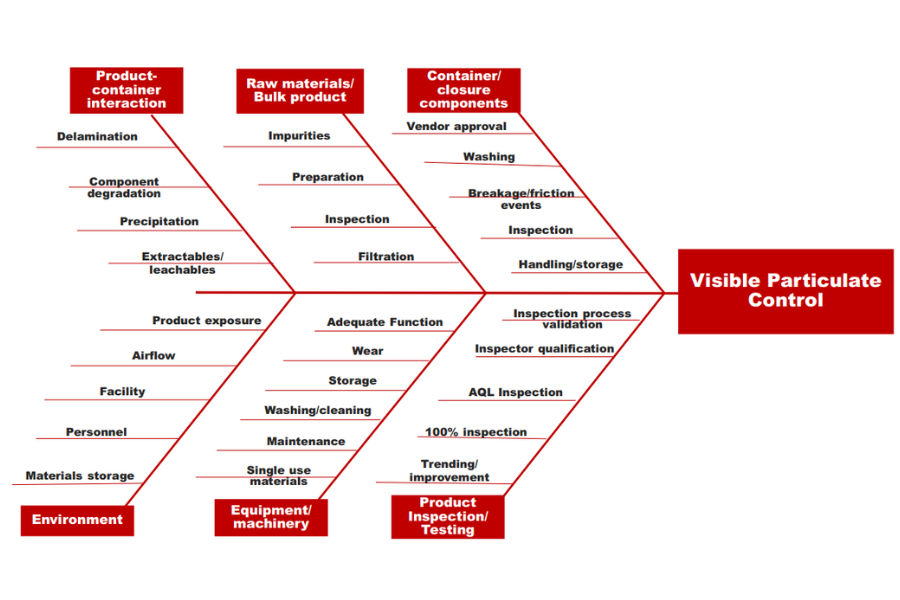
Figura 2: Exemplo de diagrama de espinha de peixe para controle de partículas visíveis. Fonte: Langille, S. E., PDA Journal of Pharmaceutical Science and Technology.
A automação desempenha um papel importante no processo de inspeção de partículas visíveis. Sistemas automatizados e semiautomatizados oferecem vantagens como aumento da produtividade, redução da mão de obra manual e uso de inteligência artificial/aprendizado profundo para melhorar o processo de inspeção. No entanto, a autora enfatiza que a seleção e validação adequadas do equipamento e processo de inspeção são essenciais para garantir a eficácia da detecção de partículas.
O cumprimento das Boas Práticas de Fabricação (BPF) é uma parte integrante dessa abordagem, com ênfase na prevenção, detecção e remediação de questões de fabricação, como contaminação por partículas visíveis. A autora destaca que a abordagem de ciclo de vida é consistente com as regulamentações da FDA e contribui para a garantia da qualidade e segurança dos produtos farmacêuticos.
O artigo também destaca a importância da prevenção da contaminação por partículas visíveis durante o desenvolvimento do produto e o processo de fabricação. Isso envolve a caracterização de partículas inerentes (características intrínsecas de alguns produtos) que podem estar presentes no produto farmacêutico.
A identificação precoce e a caracterização de partículas inerentes permitem a implementação de técnicas de inspeção visual que diferenciam essas partículas de contaminantes estranhos. Além disso, o artigo enfatiza a importância do controle do ambiente de fabricação, equipamentos e componentes para minimizar o risco de contaminação por partículas visíveis durante a produção.
A autora também aborda a importância de uma amostragem estatisticamente relevante e testes para confirmar a eficácia das medidas preventivas e do processo de inspeção de 100% na prevenção da contaminação por partículas visíveis. Ela destaca que cada lote de produto deve ser avaliado quanto à conformidade com os padrões de inspeção por partículas visíveis, conforme definido nas regulamentações. Além disso, enfatiza a importância de estabelecer limites de aceitação para defeitos críticos, maiores e menores associados à contaminação por partículas visíveis.
Em conclusão, o artigo ressalta que a aplicação de uma abordagem de ciclo de vida para o controle de contaminação por partículas visíveis em produtos injetáveis é essencial para garantir a qualidade, segurança e disponibilidade desses produtos. Essa abordagem abrangente, que se estende desde o desenvolvimento até a fabricação e inspeção, proporciona benefícios tanto para os fabricantes quanto para os pacientes, garantindo a disponibilidade de produtos farmacêuticos injetáveis de alta qualidade, seguros e eficazes.
Referências:
Langille, S. E., PDA Journal of Pharmaceutical Science and Technology September 2019, 74 359-366;
Imagem: Farma Network